|
摘要:为了从分子水平探索牦牛冷鲜肉贮藏品质特性,在冰温(-2℃)和冷藏(0℃)条件下贮藏过程中,研究牦牛肉感官品质、丙二醛含量、菌落总数和色泽的变化,利用低场核磁共振技术(low-field nuclear mag-netic resonance,LF-NMR)研究牦牛肉在贮藏过程其水分迁移规律,采用傅立叶红外光谱技术(fourier transform infrared spectroscopy,FTIR)研究牦牛肉在贮藏过程其蛋白质结构变化。结果表明:牦牛肉在冰温贮藏条件下贮藏24d仅降为“二级鲜肉”,菌落总数为5.12lg(CFU/g),而冷藏条件下贮藏至18d已为“二级鲜肉”,菌落总数为5.25lg(CFU/g)至24d已腐败变质,菌落总数为6.28 lg(CFU/g)。牦牛肉样在贮藏过程色泽红度值先上升后下降,与冰温贮藏相比,冷藏条件下降速度更显著(P<0.05)。牦牛肉丙二醛含量随贮藏时间延长逐渐增加,冷藏条件与冰温贮藏条件比较,丙二醛增加更快。上述数据表明冰温对牦牛肉的贮藏保鲜效果更好。同时,在上述两种贮藏条件下,牦牛肉中结合水含量变化趋势相同,两种贮藏条件下结合水含量差异不显著(P>0.05),不易流动水含量在冰温条件下比冷藏条件下波动小,自由水含量在冷藏条件下比冰温条件下波动小。不同贮藏条件下牦牛肉弛豫时间对应的结合水和自由水迁移明显,且冰温条件变化幅度低于冷藏条件,说明冰温条件更利于维持水分子与其他生物大分子相互作用,间接说明冰温保鲜效果更佳。对于贮藏过程蛋白质二级结构变化,冰温条件下贮藏18d后无规则卷曲相对平均含量,比冷藏条件下无规则卷曲相对平均含量低,且差异显著(P<0.05)。综合分析表明,与冷藏条件相比,冰温条件下牦牛肉结合水、蛋白质分子结构更加稳定,对维持肉生理、生化品质更为有利,因而冰温贮藏比冷藏效果更好。研究为冷鲜肉贮藏保鲜的基础研究提供新的方法参考。
关键词:水分;贮藏;品质控制;牦牛肉;蛋白质二级结构;脂质氧化
引 言
牦牛(Bos mutus 或Bos grunniens)是高寒地区的一种偶蹄、反刍、草食性稀有而珍贵的牛种,是中国相当重要的自然资源和优势资源,其主要生活于地球之巅青藏高原及其毗邻的高海拔地区,与北极熊、南极企鹅共称为“世界三大高寒动物”。牦牛肉因其肉质鲜美,高蛋白、低脂肪、低热量、营养价值高等特点,被世界各地广大消费者青睐,也成为21世纪消费的主流。
冰温保鲜技术是在冰温区域内的一种保鲜技术,继冷藏和气调贮藏后第三代保鲜技术,相对于冷冻贮藏技术,其具有不破坏细胞,很好保持肉类品质等优点。相对于普通冷藏技术,其具有更加有效抑制有害微生物的活动和各种酶的活性,可以延长冷鲜肉货架期达1.4~4倍等优点。目前冰温技术已经普遍应用于果蔬、畜禽肉类和水产品保鲜。Zhang等研究发现鸡肉采用冰温技术保鲜,相较于传统4℃冷藏保鲜,货架期延长了16d。特别在普通冷鲜牛肉保鲜方面,冰温+真空贮藏牛肉货架期达32d,而0℃+真空贮藏牛肉货架期仅8d,货架期延长了24d,可见冰温保鲜效果显著。然而,由于地域、生活习性以及品种差异,西藏牦牛肉和普通牛肉组织成分、生理生化势必存在差异,这种差异可能会影响其贮藏特性,但有关这方面报道甚少,因此有必要进一步对其进行研究。
低场核磁共振技术(low-field nuclear magnetic resonance,LF-NMR)是一种新兴的检测分析手段,具有快速、准确、无损、无侵入等特点,广泛应用于生命科学、食品农业、石油能源等的研究与应用,可对样品的水分分布信息和水分流动进行观测。目前,LF-NMR被广泛应用在果蔬干燥、植物油水分含量、鱼糜加工、肉类肌肉组织水分迁移、谷物加工等,但用于在冰温(2℃)和冷藏(0℃)条件下对牦牛肉水分迁移的影响研究鲜有报道。蛋白质是最重要的生物大分子,它的二级结构决定了其功能特性,也是检测肉品质变化的基本指标之一。检测蛋白质二级结构的方法有化学分析法、核磁共振法(nuclear magnetic resonance,NMR)、圆二色谱法(circular dichroism,CD)、傅里叶变换红外光谱(Fourier transform infrared spectroscopy,FT-IR)等。但NMR和CD具有一定的局限性,FT-IR可通过1700~1600cm-1的酰胺I区进行去卷积和曲线拟合来显示蛋白质的二级结构主成,且具有操作简单、检测速度快、所需样品少灵敏度高等优点。
本试验前期预试验测定牦牛大里脊肉冰点温度-2.4~-2.5℃,考虑到低温贮藏设备温度0.5℃波动,本试验确定2℃作为牦牛肉冰温贮藏温度。为了更好体现冰温贮藏保鲜优势,特选定冷藏温度0~4℃中最低温度0℃作为牦牛肉冷藏温度。研究牦牛肉在冰温和冷藏条件下贮藏过程中其感官评价、丙二醛含量、菌落总数和色泽影响以及应用LF-NMR、FT-IR检测其水分状态、蛋白质二级结构变化,旨在获得牦牛冷鲜肉贮藏保鲜分子机制。本研究对牦牛肉的贮藏提供一定的理论依据。
1. 材料与方法
1.1 材料与仪器
试验选取3岁左右健康西藏公牦牛,经屠宰后,胴体称质量后送入4℃冷库排酸24h,然后取大排骨相连的大里脊肉作为试验原料, PE/尼龙复合自封包装袋(透氧率<1.0%)。
Alphal-2冷冻干燥机;S400型pH计;PL203型电子天平;NMI20型核磁共振成像仪;IRTracer-100型傅里叶变换红外光谱仪;Memmert ICP110型低温培养箱。
1.2 试验方法
1.2.1 感官评分的测定
感官评分按照GB/T 22210-2008《肉与肉制品感官评定规范》进行。感官评定成员由10名专业人员组成。每次进行感官评定时将样品随机编号,随机评定,并且每个评定成员要单独进行,相互之间不能接触与交流。每次取样时先将肉样放于室温下平衡30min,然后对其色泽、气味、弹性、黏度进行评定,评定完后按表1的标准,对肉的新鲜度进行判定。
表1 鲜牦牛肉感官评分标准
|
分值
|
色泽
|
黏度
|
弹性
|
气味
|
|
2分
|
肌肉有光泽,色泽均匀
|
微干或有风干膜,不粘手
|
结构致密,手指按压后可较快恢复
|
牦牛肉特有气味,无其他异味
|
|
1~2分
|
外表色泽稍暗,切面尚有光泽
|
表面干燥或有粘手感
|
切面稍松软,按压后恢复较慢有轻微痕迹
|
有微酸味,或轻微陈腐味
|
|
0~1分
|
色泽暗淡或变色,无光泽
|
表面发干或发粘或有汁液或有霉菌
|
肉质松软,按压不能复原,有明显痕迹
|
有较明显的腐败味或臭味
|
1.2.2 理化指标、微生物指标的测定
丙二醛的测定参考GB/T 5009.181-2003的方法。
色泽的测定参照Ganasen等的方法进行。将肉样切成3cm×3cm×1cm(长×宽×厚)的小肉块。用CR-10型色差仪测定前,先将红板进行校正,检测时,对同一样品取5个点,测定其a*值(红度值),结果取平均值。
菌落总数的测定:根据国标GB4789.2—2016《食品微生物菌落总数的测定》进行。评价标准:一级鲜肉≤4lg(CFU/g);二级鲜肉4.1~6lg(CFU/g);变质肉>6lg(CFU/g)。
1.2.3 牦牛肉的贮藏与取样
在超净工作台内将牦牛肉分割成150g左右的肉块60份置于PE/尼龙复合自封包装袋中并排出袋内空气。将肉块随机分成2组,每组30袋,分别置于(0±0.2)℃、(-2±0.2)℃的培养箱中进行贮藏,培养箱相对湿度控制75%,每3d取一次样并对肉样的感官品质、丙二醛含量、相对水分含量、蛋白质结构进行测定,每个样品做3个平行试验,试验重复3次。
1.2.4 低场核磁共振法研究水分迁移
将牦牛肉切成1.0cm×1.0cm×3.0cm的条状,放入核磁管中。核磁共振仪设置参数参考Tan等的方法:T2横向弛豫时间用CPMG 脉冲序列测量,质子共振频率SF为18MHz,τ值(90°脉冲和180°脉冲之间的时间)200us,NS信号采样次数为32次,重复间隔TR时间为2000ms,回波数为4000。利用CPMG试验来检测样品的横向弛豫过程,其弛豫信号的数学表达式为:
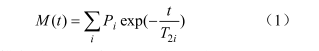
式中,M(t)为横向磁化矢量衰减到t时间后的信号量,Pi表示第i种成分的信号强度,T2i表示样品中第i种成分的横向弛豫时间(ms)。T2i区间的积分面积所占总积分面积的百分比用符号pT2i表示。
1.2.5 不同贮藏条件下样品红外光谱分析
蛋白质是最重要的生物大分子,功能特性取决于其二级结构;在FT-IR中主要有3个分析蛋白质的结构区域,称之为酰胺I区、酰胺II区、酰胺III区,分别对应1700~1600、1600~1500、1360~1200cm-1,但与蛋白质二级结构密切相关的是酰胺I区,也常被用于蛋白质二级结构的分析。本研究通过对各样品的酰胺Ⅰ谱带求二阶导数及去卷积,对各子峰进行确认,用Peakfit v4.12对曲线进行多次拟合,再根据峰面积计算来找出各二级结构的比率。各子峰与二级结构之间的对应关系为:1600~1639cm-1为β-折叠;1640~1650cm-1为无规卷曲;1651~1660cm-1为a-螺旋;1661~1700cm-1为β-转角。
利用FT-IR分析肌原纤维蛋白的二级结构。牦牛肉经真空冷冻(冷冻温度-25℃、冷阱温度-30℃,真空度20Pa)干燥48 h后粉碎成200目的粉末,准确称量2mg样品,加100mg溴化钾,用研钵研磨成均匀粉末,压制成薄片采用中红外光谱进行分析,数据收集范围在4000~500cm-1,每次测定前需扣除空气背景光谱,32次扫描积累,分辨率是4cm-1,每个样品平行测定3次,取最具代表性的图谱用于分析。
1.2.6 数据处理及统计分析
所有试验重复3次,所得数据取平均值,采用OMNIC数据处理软件处理谱图,对蛋白质在酰胺Ⅰ带(1600~1700 cm-1)波段的图谱进行分析。用Peakfit 4.12软件对谱图酰胺Ⅰ带进行傅立叶变换去卷积、二阶导数分峰拟合,GraphPad Prism7.00绘图软件作图,SPSS 21.0统计软件对数据进行处理,采用单因素方差分析(one-way analysis of variance)对结果进行显著性分析(P<0.05)。
2
结果与分析
2.1 冰温(-2℃)和冷藏(0℃)对牦牛肉感官评价的影响
感官指标是评价食品样品好坏的最直接方式,也是权衡鲜肉品质的重要指标。在2种贮藏方式下对牦牛肉的色泽、气味、弹性、黏度进行感官评定,结果见图1a。
结果表明,随贮藏时间的延长,牦牛肉感官评价呈逐渐下降的趋势,其中,0℃的样品在贮藏至18d时已经有轻微腐败味,在24d时肉样有较明显的腐败味或臭味;-2℃的样品在24d时才有轻微酸味或腐败味,2个条件下感官评价存在显著差异(P<0.05)说明冰温比冷藏的贮藏效果更佳,Jeremiah等也发现冰温比冷藏对肉保鲜效果更好。

2.2 冰温(-2℃)和冷藏(0℃)对牦牛肉色泽的影响
色泽是评判肉品质好坏的重要依据,牦牛肉在不同温度贮藏过程中,色泽的变化如图1b所示,结果表明2种贮藏温度下牦牛肉a*值先增加后降低,但冰温(-2℃)条件下a*值呈现相同变化趋势,但最终a*降低程度更少,2种贮藏温度下牦牛肉a*值变化差异显著(P<0.05)。a*值表示红度,主要来源于肌红蛋白色泽,其值越大表明牦牛肉的红色较鲜艳。因为肉样在贮藏前期表面渗透的氧气与肌红蛋白结合形成了鲜红色的氧合肌红蛋白,所以a*值升高;贮藏后期,随着贮藏时间的不断增加,pH值不断升高,氧合肌红蛋白不容易形成,使肉的颜色变暗;同时肌肉组织被氧化以及大量微生物的繁殖促进了高铁肌红蛋白的形成,高铁肌红蛋白呈褐色,所以肉色变暗,a*值下降。本结果表明冰温(-2℃)能更加有效起到预防肌红蛋白过度氧化高铁肌红蛋白,起到护色效果。
2.3 冰温(-2℃)和冷藏(0℃)对牦牛肉丙二醛的影响
丙二醛是脂质主要的次级氧化产物。过氧化的主要产物,其含量的高低可以衡量脂质过氧化的程度,脂肪的氧化程度也是评价肉品质的重要指标之一。2个贮藏温度对牦牛肉的丙二醛的影响如图1c所示,结果表明,两个温度下,随贮藏时间的延长,丙二醛含量逐渐增加,其中冷藏条件下丙二醛含量始终高于冰温条件的丙二醛含量,可能是因为铁蛋白中铁离子的释放速度受温度的影响,高温加速了铁离子的释放速度,从而加速了肌肉的氧化,使得丙二醛含量增加。在贮藏至24d结束时,0℃和-2℃贮藏条件下丙二醛的含量由贮藏前的0.53nmol/mg分别增加至1.51nmol/mg和1.19nmol/mg,差异显著(P<0.05)。冰温(-2℃)处理很大程度上降低了丙二醛的增加速率,与冷藏(0℃)相比,冰温贮藏保鲜效果更好。
2.4 冰温(-2℃)和冷藏(0℃)对牦牛肉菌落总数的影响
微生物污染导致食品营养成分分解,并产生不良气味,腐败的食品微生物则不断增加,菌落总数能直接反映微生物对食品污染程度,因此菌落总数常被用来评价食品卫生质量,可以反映肉制品的新鲜度。由图1d可知,2种贮藏方式下初始菌落总数均为3.15lg(CFU/g),随着贮藏时间的延长,菌落总数逐渐增加。在贮藏0~3d,两种贮藏方式下菌落总数无显著差异(P>0.05),贮藏4~9d过程中,冷藏条件下菌落总数显著高于冰温条件(P<0.05)。在贮藏18d时,冷藏条件下菌落总数为5.25lg(CFU/g),为二级鲜肉,冰温条件下为4.10lg(CFU/g)为一级鲜肉。贮藏至24d时,冷藏条件下菌落总数为6.28lg(CFU/g),已为变质肉,冰温条件下为5.12lg(CFU/g)为二级鲜肉,相比冷藏可延长贮藏期6d。由此得出,与冷藏(0℃)相比,冰温(-2℃)对牦牛肉的贮藏保鲜效果更好,冰温贮藏可以保鲜达24d。
2.5 牦牛肉各组分水分含量的变化
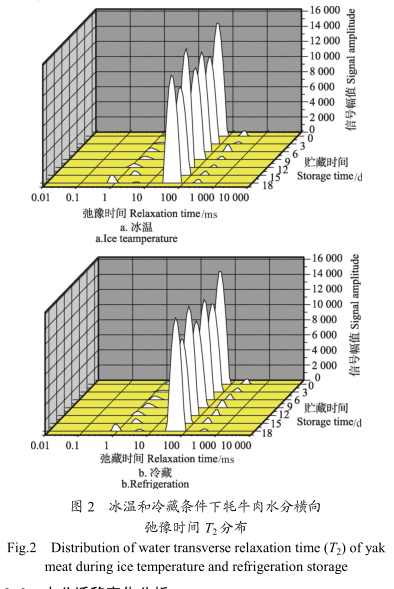
弛豫时间就是高能态的质子释放能量回到低能态所需的时间,用纵向弛豫时间(T1)和横向弛豫时间(T2)表示,通常用T2的变化以及对应的峰面积来衡量样品中水分的分布,它可以区分不同状态的水之间的化学渗透交换。如图2所示,0.01~10ms间的峰代表结合水,其与蛋白质、脂质等大分子物质紧密结合;10~100ms间的峰代表肌原纤维内截留的不易流动水;100~1000ms间的峰代表肌细胞间存在的自由水;其中,牦牛肉在2种贮藏条件下,0、3、18d均有4个峰,其余贮藏时间均有3个峰,这结果表明牦牛肉在贮藏过程中水的状态发生变化,反映了贮藏过程牛肉中水分子与其他生物分子相互作用在不断变化。在贮藏到18d时,0.01~10ms之间多了一个小峰,这可能是牦牛肉内的某些大分子物质被分解,导致结合水的流动性增强,自由度增大。同时,图2中结合水、不易流动水和自由水所处峰峰面积比例能反映三种状态水比例,通过贮藏过程峰面积的变化程度,反映肉的持水性。由图2可知,牦牛肉在冰温过程中结合水变化幅度0.25%~3.75%,自由水变化幅度0.17%~2.78%,而牦牛肉在冷藏过程中结合水变化幅度0.25%~4.25%,自由水变化幅度0.15%~3.12%,可见牦牛肉在冰温贮藏条件下持水性更高,间接反映冰温较冷藏保鲜效果更好。
表2 不同贮藏温度下牦牛肉弛豫特征中不同状态水分含量的变化
|
贮藏条件
|
贮藏时间
|
结合水
|
结合水
|
不易流动水
|
自由水
|
|
冷藏
|
0
|
0.0225±0.0048d
|
2.3101±0.0000cd
|
0.9521±0.0009ad
|
0.0223±0.0004abc
|
|
3
|
0.0133±0.0015e
|
2.5408±0.1881b
|
0.9548±0.0090ab
|
0.0193±0.0009bc
|
|
6
|
0.0267±0.0006cd
|
0.0000±0.0000
|
0.9447±0.0045b
|
0.0286±0.0004ab
|
|
9
|
0.0332±0.0033b
|
0.0000±0.0000
|
0.9437±0.0087bc
|
0.0231±0.0006abc
|
|
12
|
0.0268±0.0019cd
|
0.0000±0.0000
|
0.9552±0.0084ab
|
0.0162±0.0007c
|
|
15
|
0.0270±0.0007cd
|
0.0000±0.0000
|
0.9558±0.0034ab
|
0.0172±0.0004bc
|
|
18
|
0.0429±0.0040a
|
4.2385±0.2850a
|
0.9318±0.0041c
|
0.0202±0.0005bc
|
|
冰温
|
0
|
0.0225±0.0048d
|
2.3101±0.0000cd
|
0.9521±0.0009ab
|
0.0223±0.0004abc
|
|
3
|
0.0143±0.0009e
|
2.4254±0.1631b
|
0.9594±0.0037a
|
0.0223±0.0004c
|
|
6
|
0.0268±0.0005cd
|
0.0000±0.0000
|
0.9491±0.0055ab
|
0.0241±0.0006abc
|
|
9
|
0.0339±0.0018b
|
0.0000±0.0000
|
0.9322±0.0094c
|
0.0339±0.0008a
|
|
12
|
0.0274±0.0008cd
|
0.0000±0.0000
|
0.9505±0.0005ab
|
0.0221±0.0001abc
|
|
15
|
0.0295±0.0004bc
|
0.0000±0.0000
|
0.9449±0.0035b
|
0.0256±0.004abc
|
|
18
|
0.0337±0.0025b
|
4.2385±0.2251a
|
0.9437±0.0025bc
|
0.0147±0.0005c
|
注:同列肩标字母不同表示差异显著(P<0.05)。
本研究借助LF-NMR对肌肉中结合水、不易流动水和自由水的含量进行检测,结果如表2所示,其中,pT21、pT22为肌肉中结合水含量,pT23、pT24分别为不易流动水和自由水含量。由表可知,肌肉中水分分布发生了变化,结合水pT21、pT22在2种贮藏条件下变化趋势相同,在贮藏3d前,pT21下降,在3d后,pT21呈上升趋势,并在贮藏18d时达到最大值。在18d前,2种贮藏条件下结合水pT21、pT22均差异不显著(P>0.05),在18d时,冷藏条件下的pT21显著高于冰温(P<0.05),这是可能因为在冰温条件下水与蛋白质、脂肪等大分子物质结合得更紧密。pT23、pT24变化趋势相同,2种条件之间差异不显著。在表2中,贮藏前6d,两种条件下不易流动水、自由水相对含量基本一致,在贮藏6d后,冷藏条件下pT23比冰温条件下高,而pT24 正相反,这可能是冷藏温度促进水分从内部向表面迁移,导致冷藏条件下pT23高于冰温条件。根据pT21、pT22与pT23、pT24的变化,可以推测肌肉在贮藏过程中不同状态水之间可能存在一定的转化。
2.6 水分迁移变化分析
弛豫时间T2表征不同状态的水分流动性,弛豫时间的变化可以表明肉的水分活度的变化,T2越大,与大分子结合力小,水分自由度越大,流动性强;T2越小,流动性越差,与大分子结合越紧密,水分自由度小。
如表3所示,T21、T22表征与大分子(如蛋白质、脂质等)紧密结合的水,分别在0.83~2.31ms、2.31~4.23ms范围内波动,2个温度变化趋势相同,在贮藏15d时,T21急剧上升,这可能是在贮藏过程中,牦牛肉中与蛋白质等大分子结合的水游离出来,增加了其自由度。在贮藏12d前,冰温和冷藏随贮藏时间的延长,T21没有显著性异,在贮藏到15d时,随贮藏时间的延长差异显著(P<0.05),冷藏条件下贮藏在15d时显著高于冰温,这可能是在冷藏方式下,蛋白质被蛋白酶或微生物所分解,导致水的流动性加强,冰温抑制了酶及微生物的活性,其他时间均没有显著差异;随贮藏时间的延长,T22弛豫时间差异显著,但不同贮藏方式之间没有显著差异。说明贮藏时间增加对牦牛肉组织中结合水有一定的影响。
表3 牦牛肉弛豫时间T2随贮藏时间的变化趋势
|
贮藏条件
|
贮藏时间
|
弛豫时间
|
弛豫时间
|
弛豫时间
|
弛豫时间
|
|
冷藏
|
0
|
1.6717±0.1073b
|
2.3101±0.0000c
|
45.4485±1.3056ab
|
265.6088±0.0000b
|
|
3
|
1.5958±0.1001bc
|
2.5408±0.1631b
|
45.4485±1.3143ab
|
292.1266±1.8751ab
|
|
6
|
1.5199±0.0000bc
|
0.0000±0.00000
|
43.2876±0.0000b
|
265.6088±0.0000b
|
|
9
|
1.5958±0.1073bc
|
0.0000±0.0000
|
45.4485±1.2856ab
|
255.8038±3.5060b
|
|
12
|
1.2645±0.0812d
|
0.0000±0.0000
|
43.2876±0.0000b
|
265.6088±0.0000b
|
|
15
|
2.3101±0.0000a
|
0.0000±0.0000
|
47.6094±1.3348ab
|
265.6088±0.0000b
|
|
18
|
0.8320±0.0534e
|
4.2385±0.2880a
|
45.4485±1.3023ab
|
265.6088±0.0000b
|
|
冰温
|
0
|
1.6717±0.1073b
|
2.3101±0.0000c
|
45.4485±1.3056ab
|
265.6088±0.0000b
|
|
3
|
1.5958±0.1023bc
|
2.4254±0.1138b
|
45.4485±1.3143ab
|
292.1266±1.8751ab
|
|
6
|
1.5958±0.1078bc
|
0.0000±0.0000
|
45.4485±1.2558ab
|
278.8677±1.8751ab
|
|
9
|
1.5958±0.1073bc
|
0.0000±0.0000
|
43.2876±0.0000b
|
265.6088±0.0000b
|
|
12
|
1.4064±0.2512cd
|
0.0000±0.0000
|
43.2876±0.0000b
|
265.6088±0.0000b
|
|
15
|
2.0092±0.0000a
|
0.0000±0.0000
|
45.4485±1.3256ab
|
265.6088±0.0000b
|
|
18
|
0.8697±0.0000e
|
4.2385±0.2850a
|
49.7702±0.0000a
|
307.3712±3.4938a
|
注:同列肩标字母不同表示差异显著(P<0.05)。
如表3所示,T23代表肌原纤维内截留的不易流动水,冰温贮藏条件下T23在43.28~49.77ms范围内波动,冷藏条件下T23在43.28~47.60ms范围波动,这种波动可能是贮藏过程中,肌纤维蛋白经历分解、断裂,肌肉出现多空层,肌纤维蛋白分子量、结构变化进而影响其与水分子相互作用引起。在贮藏6d之前,冰温没有变化,贮藏6~15d之间,冰温略低于冷藏,说明冰温相对于冷藏,与大分子物质结合更紧密。
T24表示细胞间存在的自由水,这部分水最容易流失。如表3所示,T24在255.80~307.37ms范围内波动,冰温呈先上升后下降再上升趋势,冷藏呈先上升后下降再上升达到稳定状态。对于冷藏条件,在整个贮藏过程中,T24没有显著差异,始终保持较低水平。但在冰温条件下贮藏,当贮藏18d时,T24显著增加(P<0.05),冰温贮藏使牛肉保持较高自由水,从而使牛肉保持更好的嫩度。
2.7 蛋白质二级结构分析
如图3牦牛肉肌原纤维蛋白红外原始谱图所示,随着贮藏时间的延长,牦牛肉蛋白质红外光谱峰型和吸光度各有不同,说明不同的贮藏期间,其蛋白质二级结构发生了不同的变化,即不同贮藏方式、贮藏时间的蛋白质二级结构不同。
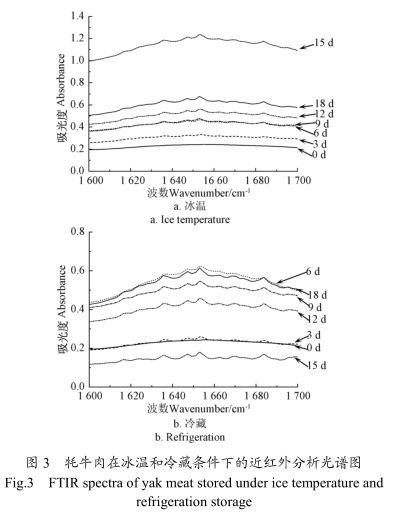
由表4可得,牦牛肉中主要以β-折叠和β-转角为主,随贮藏时间的延长,冰温条件下,β-折叠和β-转角相对含量逐渐减少,贮藏18d时增大;无规则卷曲和α-螺旋总体呈增加趋势。在冷藏条件下,β-折叠、β-转角逐渐减少,无规则卷曲和α-螺旋总体呈增加趋势,其中18d时β-折叠和β-转角相对含量分别为30.35%和30.50%。值得关注的是,在冷藏条件下,牦牛肉贮藏到15d时,其α-螺旋发生相对较大的波动,但在冰温贮藏过程中,牦牛肉α-螺旋结构变化波动较低,同时,冰温条件对新鲜牦牛肉中蛋白质β-折叠和β-转角为主的结构保持效果较好。总体而言,牦牛肉在冰温条件下贮藏,其蛋白质二级结构变化比冷藏条件下更加稳定。蛋白质是构成肉的重要品质指标之一,影响着肉的色泽和质地,特别是肉中一些生物活性酶,直接影响肉的嫩度等。由上述数据可知,相对于冷藏保鲜,牦牛肉的冰温保鲜效果更佳。
表4 牦牛肉冰温和冷藏条件下不同贮藏时间肌肉蛋白质二级结构相对含量变化
|
贮藏条件
|
贮藏时间
|
a-螺旋
|
β-折叠
|
β-转角
|
无规则卷曲
|
|
冰温
|
0
|
14.52±0.49d
|
35.24 ±1.4a
|
36.90±0.49a
|
13.33±0.39d
|
|
3
|
19.75±0.52bc
|
32.35±1.14b
|
28.57±0.52e
|
19.33±0.58ab
|
|
6
|
20.48±0.21a
|
28.71±0.75d
|
31.33±0.21b
|
19.48±0.57a
|
|
9
|
20.09±0.73ab
|
31.21±2.12bc
|
29.31±0.73bc
|
13.39±0.96d
|
|
12
|
20.00±0.26ab
|
30.87±1.39bc
|
29.78±0.26cd
|
19.35±0.77ab
|
|
15
|
20.11±0.39ab
|
30.23±1.37bc
|
30.91±0.39bc
|
18.75±0.62bc
|
|
18
|
19.76±0.22bc
|
32.52±1.09b
|
28.32±0.22e
|
19.41±0.35a
|
|
冷藏
|
0
|
14.52±0.49c
|
35.24±1.40a
|
36.90±0.49a
|
13.33±0.39d
|
|
3
|
20.12±0.32ab
|
30.60±1.78cd
|
29.77±0.32de
|
19.51±0.70ab
|
|
6
|
20.80±0.47a
|
28.21±0.50d
|
31.28±0.47c
|
19.71±0.25a
|
|
9
|
19.87±0.35ab
|
30.91±1.33cd
|
29.80±0.35de
|
19.43±0.51ab
|
|
12
|
19.84±0.52ab
|
31.85±1.16bc
|
28.98±0.52ef
|
19.32±0.53ab
|
|
15
|
15.43±0.42c
|
32.72±1.81b
|
34.57±0.42b
|
17.28±0.82c
|
|
18
|
19.88±0.50ab
|
30.35±1.30cd
|
30.50±0.50cd
|
19.27±0.25ab
|
注:同列肩标字母不同表示差异显著(P<0.05)。
结 论
冰温和冷藏两种贮藏条件下其感官评价均呈下降趋势,菌落总数和丙二醛含量逐渐增加,但冷藏条件下上述指标变化始终高于冰温条件(P<0.05),说明冰温保鲜对牦牛肉的贮藏保鲜效果更好,且比冷藏可延长贮藏期6d。牦牛肉在冰温和冷藏两种贮藏条件下结合水pT21、pT22水分含量在两种贮藏条件下变化趋势相同,但冰温条件结合水波动略低于冷藏条件,说明冰温相对于冷藏,其结合水与其他生物大分子结合更紧密。对于蛋白质二级结构,冰温条件变化幅度低于冷藏条件;贮藏18d后,冰温条件相对比冷藏条件,无规则卷曲相对含量更低,且差异显著(P<0.05),冰温条件下贮藏牦牛肉蛋白质二级结构比冷藏条件更加稳定。
综上所述,与冷藏条件相比,冰温条件下其蛋白质分子结构更加稳定,对维持肉生理、生化品质更为有利,从分子水平解释了牦牛冷鲜肉冰温贮藏比冷藏保鲜效果更好机制。本研究为冷鲜肉贮藏保鲜的基础研究提供方法参考。
|
