|
中国农业大学动物医学院孙怡朋教授课题组和吕艳丽教授课题组联合于2023年4月在eLife杂志在线发表了题为 “Increased public health threat of avian-origin H3N2 influenza virus caused by its evolution in dogs”的研究论文,揭示了犬可能作为禽流感病毒跨种感染适应人的中间宿主。
eLife杂志高级编辑、科罗拉多大学的细胞和发育生物学教授Sara L Sawyer及其同事针对该研究撰写了一篇题为“How avian influenza viruses spill over to mammals”的“Insight article”,肯定了作者在评估动物流感病毒对公共卫生安全的潜在威胁性方面的贡献,该文章同步刊发在了eLife上。

A型流感病毒频繁跨越种间障碍感染人类。犬是重要的伴侣动物,但是其在流感病毒生态中所扮演的角色还不清楚。H3N2亚型禽流感病毒在2006年前后传染给了犬,并在犬群中形成了稳定谱系。本研究自2012-2019年从中国9个省或直辖市的宠物医院及犬舍中共采集了4174份有呼吸道症状的犬的鼻咽拭子,其中235份为H3N2 犬流感病毒(CIV)阳性,病毒分离率由2012年的1.98%上升至2019年的10.85%,提示禽源H3N2流感病毒对犬的适应性显著提高。
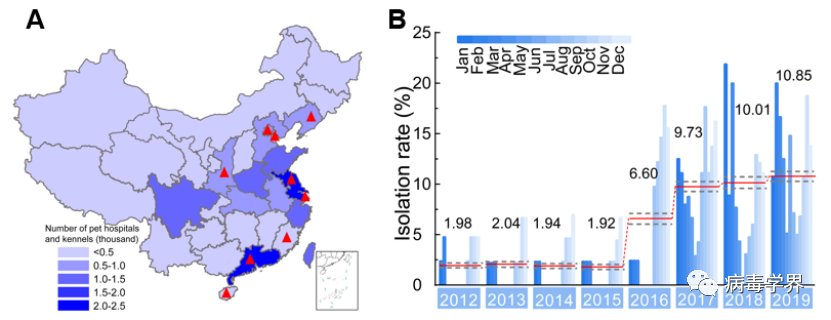
图1:H3N2 CIV采样和分离情况
A:2012-2019 年中国宠物医院和犬舍密度以及犬流感监测地点分布图;B:2012-2019 年中国犬群中 H3N2 亚型 CIVs 的阳性率。
禽源H3N2 亚型犬流感病毒(CIV)在犬群中的长期流行为研究犬对流感病毒进化的影响提供了最佳模型。研究团队进而对10多年来在世界各地分离出的H3N2 CIV的遗传演化规律和生物学特征进行了系统的比较研究。结果发现在犬中的适应,使得H3N2 CIV具备了人样受体结合能力,且血凝素(HA)酸稳定性、聚合酶活性和在原代人支气管上皮细胞(NHBE)中的复制能力也逐渐增加,在雪貂模型中还获得了100%的呼吸道飞沫传播率,H3N2 CIV对公共卫生安全的潜在威胁性增强(图2)。此外,通过基因适应性突变分析,作者还发现H3N2 CIV中与人类适应相关的氨基酸位点频率逐渐增加,并进一步确定病毒HA和PB1蛋白的氨基酸变异是导致禽源H3N2流感病毒对哺乳动物适应性提高的关键毒力因子。因此,犬可能成为禽流感病毒适应人类的中间宿主。

图2:禽流感病毒适应哺乳动物的方式
A:禽源流感病毒适应哺乳动物的方式—基因重组;B:禽源流感病毒适应哺乳动物的方式—直接感染和逐步适应;C:本文检测的H3N2 CIV与能够感染哺乳动物相关的一系列表型特性。
另外值得关注的是,作者发现人类对H3N2 CIV缺乏群体免疫力,并且从目前人类季节性流感病毒中获得的预先存在的免疫力也不能对H3N2 CIV提供保护。不过值得庆幸的是,迄今为止还没有关于人类感染犬流感病毒的报告。
中国农业大学动物医学院预防兽医系博士研究生陈明月和中国农业大学兽医教学医院吕艳丽教授为本文共同第一作者,孙怡朋教授为论文通讯作者。该研究得到国家自然科学基金(32172838和32192451)和高等教育学科创新项目的资助。
来源:病毒学界
|
