|
摘要:为了解规模猪场不同猪群的伪狂犬病病毒(PRV)感染情况及场区病毒载量分布特点,在山东省菏泽市某规模猪场,利用实时荧光定量PCR方法,对该猪场不同孕龄母猪、不同阶段生长猪群,以及各生产阶段场区环境,采集猪鼻拭子和场区环境拭子进行PRV-gE核酸检测,并对检测结果进行统计分析。结果显示:在294份猪鼻拭子中,检出42份PRV-gE核酸阳性,总阳性率为14.28%;母猪群PRV-gE阳性率为17.83%(23/129),且妊娠前后各阶段阳性率呈先上升后下降趋势,中期较高(24.00%),但差异不明显(P>0.05);不同阶段生长猪群的平均PRV-gE阳性率为11.52%(19/165),随日龄增加,阳性率也呈先上升后下降趋势,80~90日龄育肥猪最高(28.13%),与其他生长阶段猪群差异明显(P<0.05);除饲料、水源、上猪台和出猪台外,其他大部分场区环境均检测到PRV-gE核酸阳性;育肥猪群病毒载量最高,为3.6×105拷贝数/mL,其猪舍环境的病毒载量也较高,与其他环境及生长阶段猪群差异均明显(P<0.05)。结果表明,不同猪群包括免疫猪群均可遭受PRV野毒感染,尤其是母猪妊娠中期和猪育肥阶段早期,且大部分场区环境均可被污染。结果提示,规模猪场要加强各种猪群尤其是育肥猪群的伪狂犬病免疫,通过监测来调整和优化免疫程序,同时要加强生物安全,防止病毒传入和扩散。
伪狂犬病(pseudorabies,PR)是由伪狂犬病毒(pseudorabies virus,PRV)引起的,以家畜和多种野生动物发热、奇痒及脑脊髓炎为特征的急性、热性传染病,呈世界性分布。猪是PRV的天然宿主,因此PRV对养猪业危害最为严重。感染PRV后,妊娠母猪可出现产木乃伊胎或死胎等流产症状;不到7日龄的仔猪,以无明显临床症状的突然死亡为特征;2~3周龄仔猪可出现严重的中枢神经症状,死亡率可高达100%;保育猪可出现神经症状和呼吸道症状,致死率为10%~20%;生长猪和育肥猪可出现呼吸道症状,常因继发细菌性肺炎而死亡。2011年以后,PR在我国从北向南又出现了新一轮流行,到2017年全国各地仍时有PR暴发和流行,造成了严重经济损失。本研究检测分析了山东省菏泽市某规模化PRV阳性猪场不同猪群感染情况,以及不同生产阶段和场区环境中的病毒分布情况,以期为规模化猪场的PR免疫及生物安全防控提供依据。
材料与方法
猪场发病概况
该猪场存栏母猪约1 000头。2019年9月育肥猪首先出现呼吸困难、体质量下降、咳嗽等症状,死淘率近8%;随即保育猪出现咳嗽、四肢划水、被毛粗乱、精神萎靡等临床特征,死淘率约10%。之后逐渐波及产房,新生仔猪无明显临床症状死亡,2~3周龄仔猪出现战栗、惊厥、震颤、四肢划水等神经症状,病死率达15%,同时妊娠舍怀孕母猪出现流产(产木乃伊胎、死胎)以及呼吸道症状和高烧等特征,流产率约10%。该场PR疫苗免疫程序见表1。

为查明原因,在猪场发病后立即采集20份病料(育肥猪4份、仔猪8份、流产胎儿8份),采用荧光定量PCR方法,进行猪瘟病毒(CSFV)、猪繁殖与呼吸综合征病毒(PRRSV)、PRV、猪圆环病毒2型(PCV2)、猪流行性腹泻病毒(PEDV)检测。根据检测结果,结合临床症状,判断PRV是引起猪场发病的主要原因。随后对PRV-gE基因进行测序。遗传进化分析显示,该规模化猪场中流行的PRV属于2.3型变异野毒株。
样品采集
为进一步调查PRV在该规模化猪场各猪群中的感染情况、场区环境分布情况及病毒载量,随机采集猪场临床健康猪只鼻拭子(因鼻腔的PRV滴度效价较高),包括:母猪鼻拭子129份,其中断奶后20份、妊娠前期(<30 d)22份、妊娠中期(31~85 d)25份、妊娠后期(86~114 d)30份、哺乳期32份;仔猪(15~21日龄)鼻拭子50份,保育猪(45~50日龄)鼻拭子25份;育肥猪鼻拭子90份,其中80~90日龄32份、120~130日龄30份、160~180日龄28份;场区环境样本拭子,包含圈舍、饲料、水源、粪便等各5份。将采集的新鲜拭子样本,使用灭菌生理盐水悬浮。样本收集后,若不能即时检测,则2~8 ℃冷藏过夜保存;若长期保存,则-80 ℃冷冻保存。
检测及分析
采用PRV-gE基因荧光定量PCR检测试剂盒(武汉科前生物股份有限公司产品),按照试剂盒使用说明进行检测。结果判定:Ct≤35或有明显指数增长期,为阳性;Ct值在35~38范围内,则对标本进行重复检测,若Ct值仍在35~38范围内,且有明显指数增长期,为阳性,反之为阴性;Ct>38或无Ct值,为阴性。将标准品Ct值与浓度制作成标准曲线,然后依据待检样品Ct值计算待检样品浓度,并换算成拷贝数。采用Excel软件对试验数据进行处理,使用SPSS 19.0软件,对检测结果进行加权处理后实施卡方检验,显著水平为P<0.05。
结果与分析
母猪群检测
检测结果(表2)显示:母猪群PRV-gE平均阳性率为17.83%,妊娠前后各阶段表现为先上升后下降趋势,其中妊娠中期最高,为24.00%。经SPSS卡方检验,各阶段阳性率差异不明显(P>0.05)。
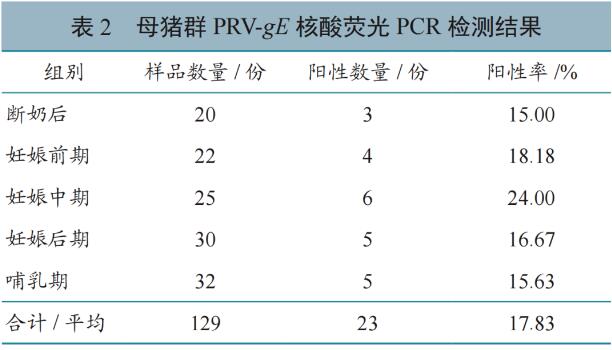
生长猪群检测
检测结果(表3)显示:生长猪群PRV-gE平均阳性率为11.52%,且随日龄增长呈现急速上升又快速下降趋势,其中80~90日龄育肥猪阳性率最高,为28.13%,经SPSS卡方检验,与其他日龄段猪群差异显著(P<0.05)。
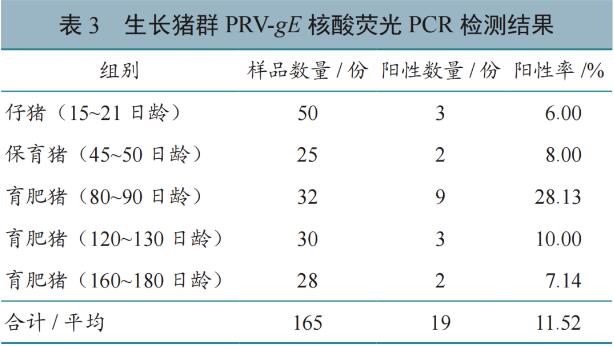
不同生产阶段场区环境及猪群病毒载量检测
检测结果(表4)显示:饲料、水源、上猪台和出猪台样品中未检测到PRV-gE阳性,而妊娠舍(粪沟、限位栏表面、妊娠母猪),产房(粪沟、产床表面、分娩舍底部、哺乳母猪、仔猪),保育和育肥舍(圈舍栏表面、保育猪、育肥猪)样品中均检测到PRV-gE阳性;育肥猪群带毒量最高,为3.6×105拷贝数/mL,经SPSS卡方检验,与其他环境及猪群样品差异均显著(P<0.05)。
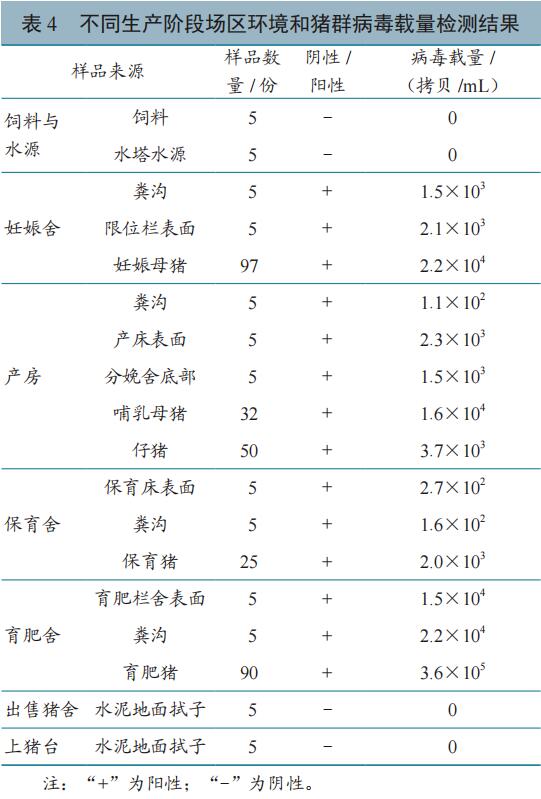
讨论
PR流行给国内养猪业带来了巨大经济损失。2012年以后,我国各地Bartha-K61疫苗免疫猪群也发生过大规模PR疫情或处于野毒感染状态,导致种猪繁殖障碍,仔猪死亡率升高。Gu等对山东省2013—2016年采集的2 033份血清抗体进行检测,发现PR野毒抗体阳性率为57.8%;张晓阳对山东省2018年采集的5 038份血清抗体进行检测,发现gE抗体总体阳性率为45.00%。上述结果表明,PRV变异毒株已经在山东省广泛流行,并持续感染。另有研究表明,Bartha-K61疫苗对分离到的PR毒株仅能提供50%的交叉保护。Zhou等在山东省某猪场的研究结果表明,免疫Bartha-K61毒株疫苗后,仍然出现仔猪顽固性腹泻、神经症状以及母猪流产、产死胎等症状。该猪场免疫疫苗同样为Bartha-K61,仍然发生PR野毒感染,表明Bartha-K61疫苗不能完全抵御野毒入侵。
杨涛等在分子生物学水平上比较了PRV Bartha-K61疫苗株与当前流行的变异株之间的差异,发现疫苗株和变异株分属于不同的分支。古金元等和刘照虎等分别对山东省不同地区的规模猪场进行了PRV分离,发现分离株与国内报道的PRV变异株核苷酸同源性均高于欧美毒株,与疫苗株Bartha-K61株遗传距离较远。这进一步解释了该猪场免疫的Bartha-K61疫苗株不能对变异株提供充足保护的原因。
PR发生后,为探究该猪场不同猪群感染情况,以便为后期疫苗免疫程序优化和生物安全防控提供数据支撑,本研究检测了不同猪群的鼻拭子样品,发现病原总体阳性率为14.28%。张树金等在2015—2017年对山东省PRV流行情况进行调查,发现PRV平均抗原阳性率为12.30%。刘照虎等在山东省进行PR检测分析,发现2017年、2018年的病原阳性率分别为11.20%、7.54%。该猪场检出的PR病原阳性率较高,说明本场PRV感染较为严重,当然也可能与本次检测样本量较小有关,后需进一步扩大检测样本量。对生长猪群进行PRV检测时发现,不同生长猪群间的病原阳性率有差异,其中育肥猪显著高于其他日龄段。这一方面和该场使用的Bartha-K61疫苗株与变异株同源性较差,交叉保护力不足有关;另一方面可能是二免日龄过早(35日龄),受母源抗体干扰,导致75日龄二次加强免疫效果较差,产生保护力不足。在对妊娠母猪群进行PRV检测发现,妊娠母猪群间的病原阳性率差异不明显,但妊娠中期略高。张嘉保等在对妊娠母猪细胞免疫水平的研究中发现,妊娠中期免疫抑制作用较强(差异不显著)。另有研究表明,妊娠可以使病毒活化,增加感染PRV的潜在风险,且孕期的胎盘传播,主要从怀孕中期开始。本研究发现,母猪妊娠中期病原阳性率较高,这可能与母猪妊娠中期的免疫抑制有关。
鼻腔黏膜和口腔是PRV感染的主要入侵部位。研究表明,感染PRV猪的分泌物、排泄物和呼吸物中都有较高的病毒载量,且病毒对外界环境具有较强的抵抗力。本研究发现,除饲料、水源、上猪台、售猪台外,不同猪群及各阶段生产环境中均可检测到PRV,且猪群带毒量越高,相应环境中的病毒载量就越高。这进一步说明该猪场PRV的传播主要通过猪与猪的直接接触,或是与PRV污染的感染物相接触。故严格执行场区各生产阶段的有效隔离,加强消毒处理,对于防止PRV传播尤为重要。
综上,该规模猪场不同猪群均遭受PRV不同程度的感染,尤其是母猪妊娠中期和育肥猪早期,且大部分环境中均能检测到病毒。因此,规模猪场要加强PRV监测,通过监测来调整优化PR免疫程序,同时要加强生物安全控制,进行系统性防控。
|
