|
为了研究腹水综合征(AS)肉鸡肝脏缺氧诱导因子-1α(HIF-1α)基因的表达与肌成纤维细胞(MFB)数量变化之间的关系,本试验采集5只10周龄AS肉鸡及5只健康肉鸡肝脏,切取一部分以10%的福尔马林固定,大部分置于-80℃冰箱保存,采用石蜡切片技术进行HE染色及免疫组化技术对肉鸡肝脏进行显微结构和α-SMA蛋白的表达及分布情况的观察,用qRT-PCR技术对HIF-1α基因进行检测。结果显示:AS肉鸡肝脏结构排列松散,HIF-1α基因表达极显著(P<0.01),α-SMA蛋白含量表达显著(P<0.05)。本试验结果表明:腹水肉鸡肝脏HIF-1α基因含量表达及α-SMA蛋白含量表达相比健康肝脏均显著增多,肝星状细胞被HIF-1α基因刺激激活,合成分泌α-SMA蛋白,进而转化为具有增生性和纤维原性的MFB细胞,HIF-1α基因的表达量与MFB细胞的增多成正比。
关键词:肉鸡;腹水综合征;HIF-1α;α-SMA;MFB;肝脏;纤维化;肉鸡腹水综合征(ascites syndrome,AS)是缺氧引起的以腹水、肺脏动脉高压和右心衰竭为主要特征的临床综合征[1]。AS肉鸡剖检显示肝脏充血肿大或皱缩,表面凹凸不平,颜色多呈暗红色,常有棕黄色沉积物,肝脏周围有淡黄色或灰白色胶冻状凝块附着,肝静脉和门静脉怒张充血[2]。AS肉鸡心脏功能不全导致肝脏缺乏有效的循环血量和供氧,加重肝损伤最终发生纤维化,引起腹水。缺氧诱导因子-1(hypoxia-inducible factor-1,HIF-1)作为在缺氧条件下主要的调节因子起着关键作用[3][9],缺氧诱导因子-1α(HIF-1α)是HIF-1主要的氧调节亚基,决定其水平及活性。肝纤维化是多种原因引起的反复和慢性肝损伤造成细胞外基质(extracellular matrix,ECM)积累的病理现象。目前研究认为,肝纤维化的ECM主要由肝星状细胞(hepatic stellate cells,HSC)合成[4],HSC在肝纤维化的发生、发展和逆转过程中起至关重要的作用[5]。当肝脏受到损伤时,HSC表型会发生变化,通过激活α-平滑肌肌动蛋白(α-smooth muscle actin,α-SMA)转化为肌成纤维细胞(MFB),生成大量ECM[6,10]。试验通过对AS肉鸡肝组织中α-SMA蛋白的表达量进行测定,进而观察出MFB细胞分布的数量,同时对HIF-1α基因表达含量进行测定,初步探索AS肉鸡肝脏HIF-1α基因的表达与MFB细胞数量的变化关系。
1 材料与方法
1.1 试验材料
试验所用鸡采集于新疆阿克苏市郊某肉鸡养殖场,为10周龄健康肉鸡和AS肉鸡。
主要试剂:平滑肌肌动蛋白多克隆抗体兔抗鸡一抗、免疫显色试剂Poly-HRP羊抗小鼠/兔二抗试剂购自武汉三鹰生物技术有限公司,苏木素、伊红、0.01M柠檬酸钠缓冲试剂(p H6.0)购自北京索莱宝科技有限公司,HIF-1α抗体购自北京博奥森生物技术有限公司,HRP-DAB底物显色试剂盒购自天根生化科技有限公司,(Trans Zol Up Plus RNA Kit)RNA提取试剂盒、反转录试剂盒、Green q PCR Super Mix试剂盒购自北京全式金生物技术有限公司。
主要仪器:石蜡包埋机(EG1150)、手动切片机(RM2125)购自Leica德国,生物显微镜(尼康E200)购自尼康江南光学仪器有限公司,实时荧光定量PCR仪Quant Studio 5购自美国默飞世尔科技公司,梯度PCR仪TC-5000购自法国TECHNE。
1.2 试验方法
1.2.1 样本的采集和保存
取5只10周龄肝脏腹水肉鸡和5只10周龄健康肉鸡的肝脏组织样本,一部分以10%的福尔马林固定;另一半置于-80℃冰箱保存。
1.2.2 肝脏的显微结构特征观察
10%福尔马林固定的样品,经石蜡包埋,切取5μm厚度切片放置60℃恒温箱烘烤1 h,经二甲苯脱蜡、梯度酒精复水、苏木精-伊红染色后,再经梯度酒精脱水后用中性树胶封片,通过光学显微镜观察肝脏结构的微细结构变化。
1.2.3 利用免疫组化研究肌成纤维细胞的分布
烤片:将已完成的切片在60℃条件下烘烤1 h。
脱蜡:将烘干后的切片在二甲苯溶液中脱蜡两次,每次约10 min。
梯度水化:将浸泡后的切片依次置于无水酒精、95%、85%、75%酒精溶液中浸泡,每一次均约5 min,最后将切片置于蒸馏水中漂洗约5 min。
热修复抗原:取枸橼酸盐缓冲液0.01M,将漂洗后的切片浸入,并置于微波炉中加热,沸腾后断电,10 min后再次低火煮15 min,静置待其冷却后用p H为7.2~7.6的PBS冲洗3次,每次约3 min。
阻断:每张切片加50μL 3%过氧化氢溶液,放置约15 min以使内源性酶失去活性,PBS洗涤3次,每次约5 min。
孵育一抗:向切片上滴加一抗(smooth muscle actin Polyclonal antibody),并置于4℃冰箱中,12 h后取出切片,经PBS洗涤3次,每次5 min。
孵育二抗:滴加50~100μL免疫显色试剂Poly-HRP羊抗小鼠/兔二抗试剂,37℃烤箱中放置30 min,PBS液洗涤3次,每次5 min。
DAB显色:滴加预制好的DAB工作液50~100μL,5 min后镜下观察染色情况并控制反应时间,染色后用蒸馏水洗涤。
苏木素染液浸染5 min,用蒸馏水洗涤后,经PBS返蓝。
梯度溶液(60%~100%)脱水,每级约5 min。取出后将切片置于二甲苯溶液中处理两次,每次约10 min,最后滴加中性树胶封片[7]。通过光学显微镜观察a-SMA蛋白在腹水肉鸡肝脏中不同部位的分布和比例。注:以PBS代为一抗作为阴性对照。
1.2.4 HIF-1α的表达及蛋白含量检测
引物设计:HIF-1α引物参照韩烨晨等的报道[8],GAPDH通过Primer Premier 5.0软件进行引物设计,由上海生工合成。
肝组织RNA的提取:使用RNA提取试剂盒(Trans Zol法)进行提取,并用Nanodrop测定RNA浓度。
肝组织RNA的反转录:用Two-Step反转录试剂盒合成c DNA;依次加入Total RNA 1μL、Anchored Oligo(d T)18 Primer(0.5μg/μL) 1μL、2x ES Reaction Mix 10μL、Easy Script?RT/RI Enzyme Mix 1μL,g DNA Remover 1μL、RNasefree Water 6μL,总体积20μL。将20μL体系放于PCR仪中反应15 min(42℃),85℃加热5 s,产物于-20℃保存。
实时荧光定量PCR:将反转录产物c DNA浓度稀释10倍,取稀释后c DNA,Green q PCR Super Mix试剂盒说明书进行操作。依次加入c DNA1μL、Forward Primer 0.4μL、Reverse Primer 0.4μL、2x Perfect Start?Green q PCR Super Mix 10μL、RNase-free Water 8.2μL,总体积20μL。反应条件为:95℃30s;95℃15 s;60℃30 s;溶解曲线为95℃15 s;60℃1 min;95℃1 s;40个循环,每个样品做三个生物学重复试验,根据每个样品的Ct值用2-ΔΔCt公式计算HIF-1α的m RNA在腹水肉鸡肝脏中的相对表达量。HIF-1α基因引物序列见表1。

1.2.5 数据分析
q RT-PCR用Graph Pad Prism8.0作图,免疫组化用Image J 1.8.0进行分析。数据用SPSS22.0软件进行分析,结果以“X±S”表示,以P>0.05表示差异不显著,P<0.05表示差异显著,P<0.01表示差异极显著。
2 结果与分析
2.1 肝脏的HE染色
结果显示如图1。与健康肉鸡肝组织(图1A)相比,腹水肉鸡肝组织(图1B)完全失去正常结构,肝索排列松散,部分正常肝细胞结构被破坏;肝血窦变大并淤血。出现部分炎性细胞及成纤维细胞。

2.2 肝脏α-SMA的表达量
结果显示如图2。与对照组相比,腹水组α-SMA表达更明显。对肝脏组织进行阳性面积测定,结果显示腹水组(图2B)阳性面积比值是(12.70±1.65)%,健康组(图2A)为(0.54±0.36)%,差异显著(P<0.05)。

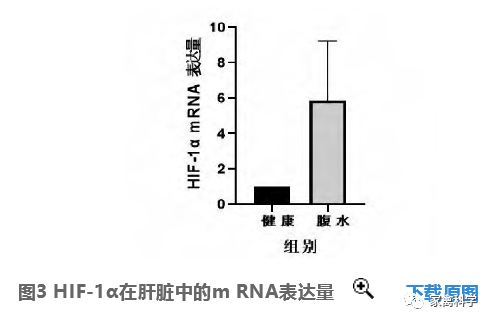
2.3 HIF-1α的表达量
结果如图3。q RT-PCR结果显示,HIF-1α在腹水肉鸡肝脏差异表达极显著(P<0.01)。
3 讨论
研究表明,患有腹水综合征的肉鸡肝脏损伤严重[15]。HIF-1α是在于哺乳动物细胞质内的转录因子,也是引发AS肉鸡的关键因子[16],在低氧环境中,HIF-1α在细胞内积聚并与HIF-1β结合形成HIF-1,HIF-1与缺氧反应原件(HRE)结合,参与多条信号转导通路,引起细胞对缺氧的反应[17]。在本试验中,腹水肉鸡肝脏HE染色显示肝组织完全失去正常结构,肝索排列松散,部分正常肝细胞结构被破坏;肝血窦变大并淤血,与健康肉鸡肝脏显微结构差异明显,与李凯的研究结果一致[14]。肉鸡腹水综合征是一种由遗传、营养[18]、环境[19]等多因素导致的营养代谢病,但是缺氧是腹水肉鸡发病的重要因素[20]。前期研究表明,AS肉鸡剖检显示肝脏充血肿大或皱缩,表面凹凸不平,颜色多呈暗红色,常有棕黄色沉积物,肝脏周围有淡黄色或灰白色胶冻状凝块附着,肝静脉和门静脉怒张充血[2]。这是因为AS肉鸡心脏功能不全,继而导致肝脏缺乏有效的循环血量和供氧,加重肝损伤,最终发生纤维化,引起腹水。q RT-PCR结果显示腹水肉鸡的肝脏中HIF-α基因表达极显著(P<0.01)高于健康肉鸡,说明在低氧环境中,肉鸡体内HIF-1α被激活。肝星状细胞(HSC)在肝纤维化过程中起着重要作用,正常为静息状态,当受到外界因子刺激时,合成分泌平滑肌动蛋白(α-SMA)进而转化为肌成纤维细胞(MFB)[11][12],因此,MFB水平的变化与肝脏纤维化水平呈正相关。本研究结果显示,腹水肉鸡肝脏α-SMA蛋白含量表达显著(P<0.05)高于健康肉鸡,与韩烁晨的研究结果一致[13],这表明在AS发病过程中,MFB参与肝脏的纤维化形成。
4 结论
在AS肉鸡形成的过程中,HIF-α表达均持续升高,肝星状细胞被HIF-1α基因刺激激活,合成分泌α-SMA蛋白,进而成为具有增生性和纤维原性的MFB,导致细胞外基质过度沉积,器官纤维化形成。腹水肉鸡肝脏HIF-α含量及α-SMA含量表达均显著高于健康肉鸡(P<0.01,P<0.05),且HIF-1α基因的表达量与MFB细胞的增多成正比。
|
